今年的 ESMO 年会在西班牙马德里召开。疫情之后,会议的重心重新放到了线下,虽然在线上还是给注册用户提供了视频直播和回放,以及壁报浏览服务,但到现在为止还没提供幻灯片和壁报的下载,有些遗憾。按照惯例,这里还是总结一下今年个人认为比较重要的研究,做一下分享,分为肝细胞癌(HCC)和胆道系统肿瘤(胆管癌,BTC)两个部分。

肝细胞癌(HCC)的系统治疗
Ociperlimab(TIGIT 抗体)用于晚期肝癌一线治疗的 II 期研究(AdvanTIG-206)(945MO)
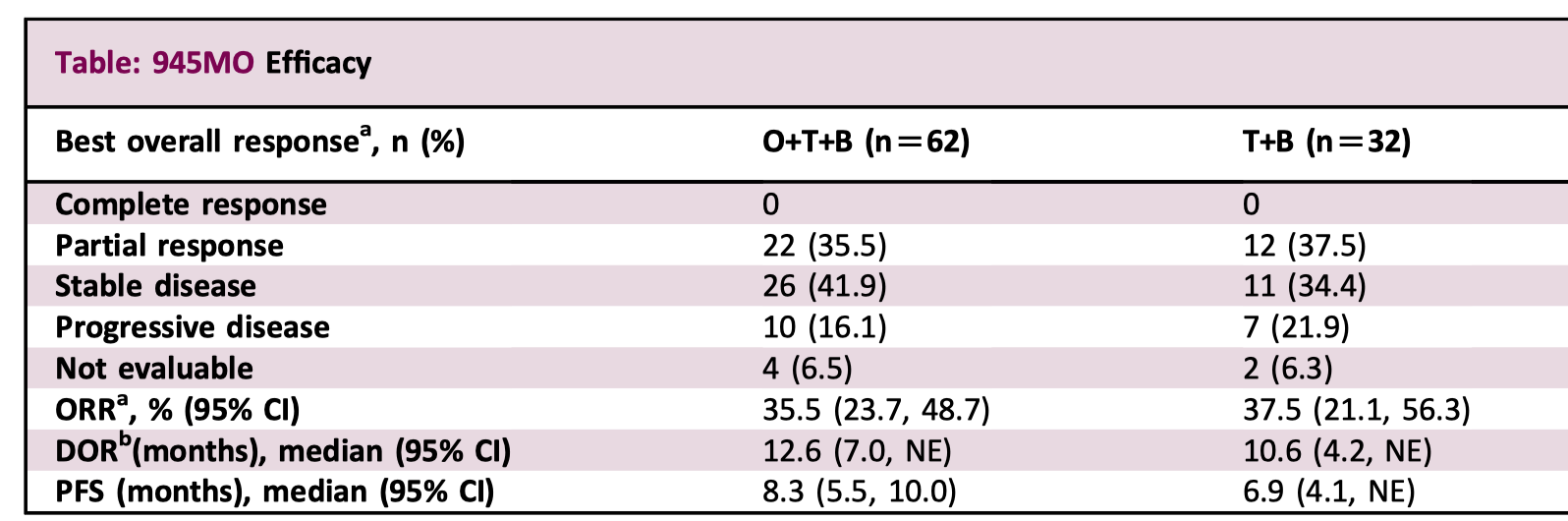
今年年初的 ASCO 年会上,罗氏公司报道了他们家的 TIGIT 抗体(tiragolumab)用于晚期肝癌一线治疗的 II 期研究(Morpheus-Liver 平台)的结果。在阿替利珠单抗和贝伐珠单抗(T+A 方案)的基础上,增加 tiragolumab 可进一步提高疗效,并且不良反应没有明显增加,目前 III 期随机对照研究(IMbrave152)也已经正在入组受试者。但那项 II 期研究存在不少值得推敲之处,个人对 TIGIT 抗体能不能给现有治疗增效还存在疑问。因此,百济神州的这项设计相似的 II 期研究让我非常期待。 在这项叫做 AdvanTIG-206 的 II 期研究中,92 例未经系统治疗的晚期肝癌患者按照 2:1 的比例随机接受 ociperlimab(TIGIT 单抗)联合替雷利珠单抗和贝伐珠单抗(Tis/Bev)三药治疗或 Tis/Bev 二药治疗。结果显示(下表),在增加了 ociperlimab 之后,ORR 和 PFS 都没有得到改善,SD 的比例有所提高,因此 PD 有一些下降。而 ociperlimab 似乎还带来了更多的不良反应,≥3 级的治疗相关不良事件(TRAE)在三联和二联治疗组中分别为 50.0% 和 25.8%。这样一来,TIGIT 抗体的疗效就显得更加扑朔迷离了,前面有一篇文章中,我也谈了一些个人想法。
仑伐替尼联合纳武利尤单抗用于晚期肝癌一线治疗的II期研究(IMMUNIB)(955P)
这是在德国开展的一项单臂研究,评估的是两者联合用于晚期肝癌的一线治疗。总共入组了 50 例患者,其中近一半是 BCLC B 期,1/3 是 C 期。疗效方面,ORR 32%(RECIST v1.1 标准),PD 发生率 12%,中位 PFS 9.0 月,中位 OS 25.4 月,≥G3 TRAE 的发生率 59%。 整体而言,这些疗效和安全性数据都符合预期,因为仑伐替尼跟各家 PD-1 抗体联合都显示出相似的抗肿瘤活性。目前,III 期的随机对照研究 [[LEAP-002]] 显示,在仑伐替尼的基础上增加帕博利珠单抗只在数值上延长了 OS 和 PFS,但没有达到预设的统计学差异,非常遗憾。但仑伐替尼联合 PD-1 抗体的疗效经受住了反复的临床验证,并且,增加 PD-1 抗体还可以推迟患者生活质量恶化,因此个人认为,两者联合依然可以作为一线治疗的有效选择。
仑伐替尼联合卡度尼利单抗用于晚期肝癌一线治疗的 Ib/II 期研究(947P)
卡度尼利单抗是一个靶向 PD-1/CTLA-4 双特异性抗体,跟 PD-1 抗体相比,增加了对 CTLA-4 靶点的抑制作用,理论上讲疗效数据可能会更好。这项研究总共入组了 59 例未经系统治疗的中晚期肝癌患者,按照卡度尼利单抗用药方案不同分为 A(n=31)和 B(n=28)两个队列,分别接受 6 mg q2w 和 15 mg q3w 的用药。主要终点方面,A 和 B 队列的 ORR(RECIST v1.1 标准)分别为 35.5% 和 35.7%,中位 PFS 分别为 8.6 和 9.8 月,其他疗效数据见下表。跟仑伐替尼联合 PD-1 抗体的历史数据比起来,联合卡度尼利单抗的疗效数据似乎稍一点。安全性方面,≥G3 的 TRAE 发生率 66.1%,也算是可以接受的水平。
值得一提的是, 卡度尼利单抗用于多瘤种的 I 期研究 COMPASSION-03 近期发表了 00411-4/fulltext)。 该研究也初步评估了这个药物用于晚期肝癌单药治疗的疗效和安全性。入组了 24 例肝癌患者,其中 7 例(29%)此前未接受过抗肿瘤治疗。疗效方面,ORR 16.7%,DCR 62.5%。安全性方面,3-4级 TRAE 29%。从这些数据看起来单独使用卡度尼利单抗的疗效数据跟一般的 PD-1 抗体相似,这项研究没有体现出双特异性抗体的优势,安全性方面看起来又稍差一些。当然,这个初步研究的样本量很小,下结论为时过早。
恩沃利单抗联合 suvemcitug 用于肝癌的后线治疗的 II 期研究(959P)
恩沃利单抗是一个皮下注射的 PD-L1 抗体,suvemcitug 则是一个 VEGFA 抗体,有些类似于贝伐珠单抗。这项 II 期研究入组的是至少接受过一线系统治疗的晚期肝癌患者。目前入组了 20 例患者,其中 16 例接受过一线治疗,8 例接受过免疫治疗。在可评估疗效 18 例患者中,ORR(RECIST v1.1 标准)为 11.1%,DCR 72.2%,中位 PFS 为 4.3 月。整体而言,将 VEGFA 抗体联 PD-1/PD-L1 抗体用于后线治疗具有一定的抗肿瘤活性,但疗效相对有限。
Sitravatinib 联合替雷利珠单抗用于晚期肝癌的 Ib/II 期研究(SAFFRON-104)(948P)
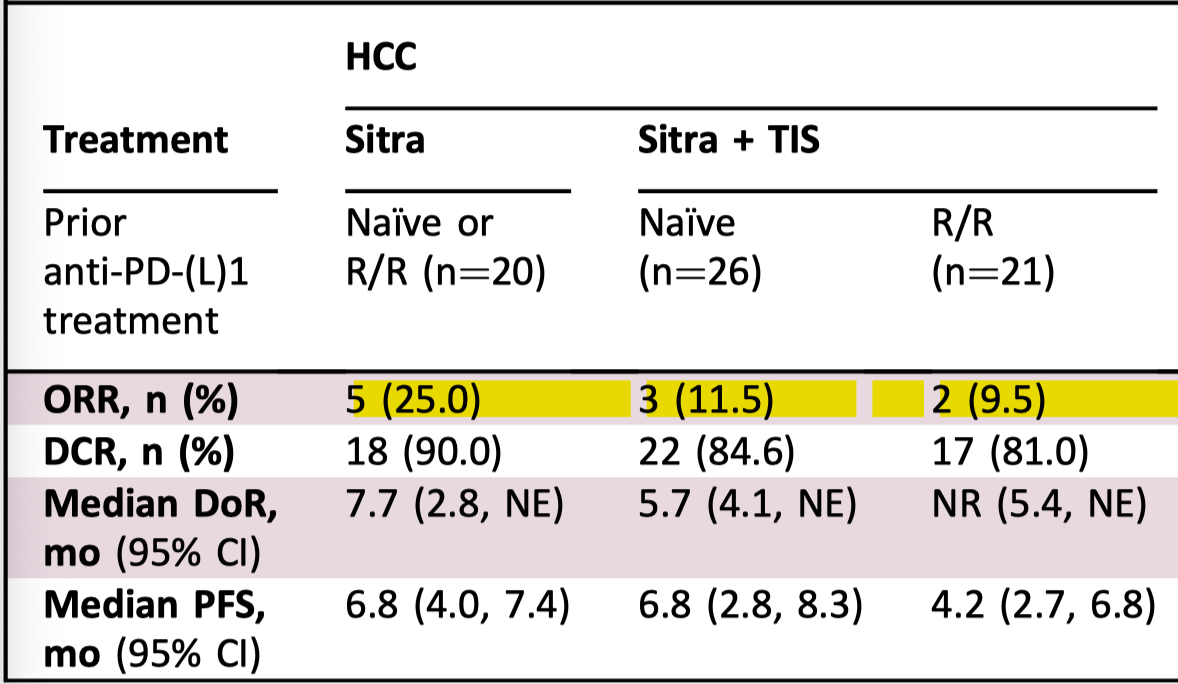
Sitravatinib 是一个小分子的多靶点酪氨酸激酶抑制剂。这项叫做 SAFFRON-104 的研究入组的患者比较复杂,我主要关注扩展队列的疗效数据,其中包括了一个肝癌的队列。未经免疫治疗或免疫治疗耐药的 20 例肝癌患者接受 sitra 治疗,ORR(RECIST v1.1 标准)为 25%,DCR 为 90%,中位 PFS 6.8 月。在未经免疫治疗的 26 例患者,接受 sitra 联合替雷利珠单抗治疗,ORR 11.5%,DCR 84.6%,中位 PFS 6.8 月;免疫治疗耐药的 21 例患者,ORR 9.5%,DCR 81%,中位 PFS 4.2 月。接受 sitra 单药治疗或者 sitra 联合替雷利珠单抗治疗的 ≥3 级 TRAE 发生率分别为 44.6% 和 54.2%。看起来 sitra 单药或者跟免疫治疗联合显示出了一定的抗肿瘤疗效,但从 ORR 数据看,两者联合使用并未出现 1+1≥1 的效果,不知道公司方面有没有动力将这个组合推进到 III 期对照研究。
T+A 方案进展后治疗的亚太地区的真实世界研究(970P)
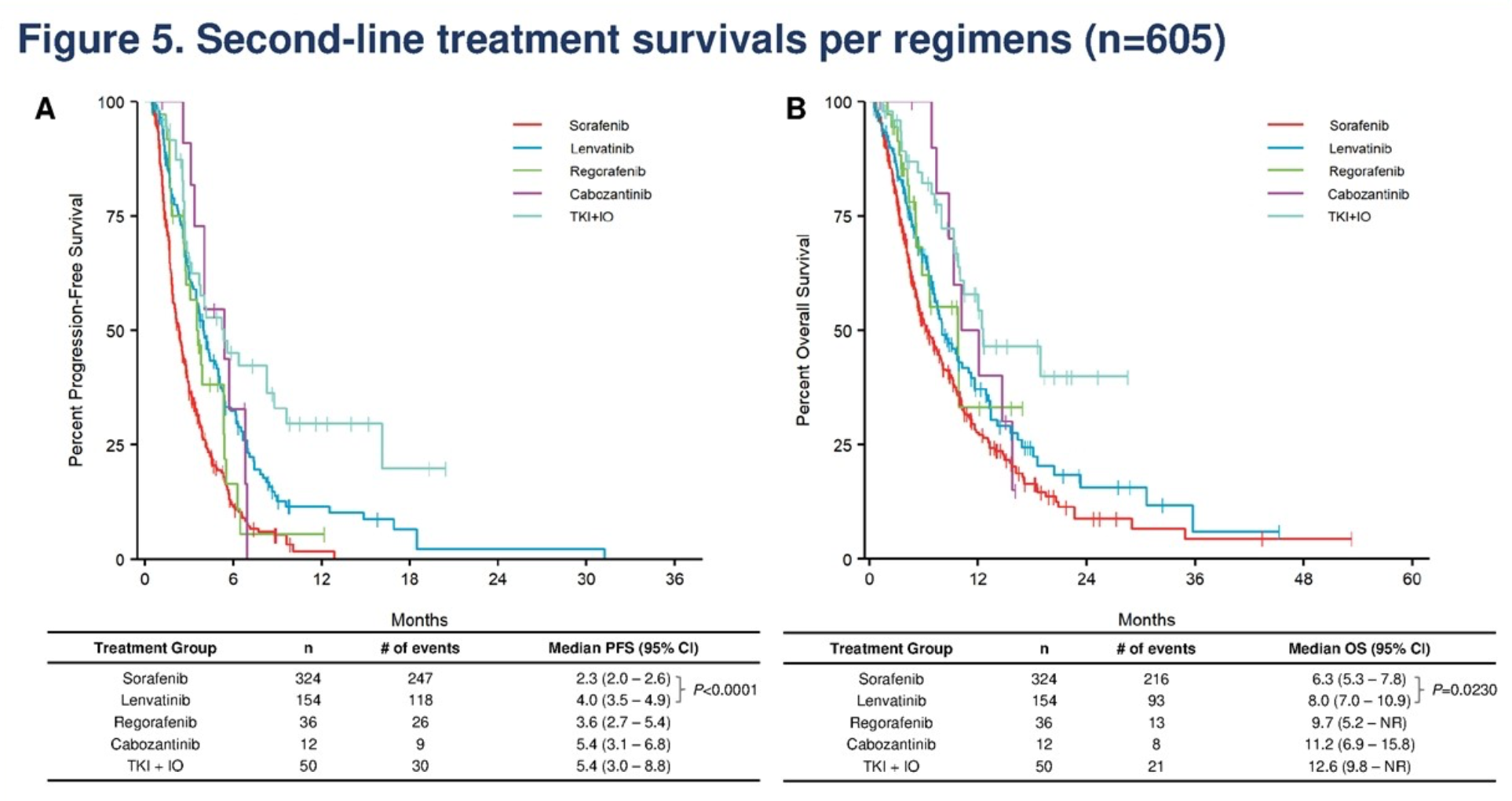
目前获批的晚期肝癌二线治疗药物都是基于索拉非尼(部分是化疗)治疗失败后的患者来开发的,但目前晚期肝癌的一线治疗的方案已经发生了改变,其中 T+A 方案是国际上最受认可的治疗方案。T+A 进展后该如何选择目前没有定论,也缺乏前瞻性研究的数据。这项在韩国、泰国、新加坡、香港和台湾等地开展的真实世界研究,入组了 T+A 治疗失败后接受了后线治疗的患者共 369 例。这些患者中接受索拉非尼和仑伐替尼治疗的比例最多。与索拉非尼相比,仑伐替尼可获得更长的 PFS(3.7 vs 2.1 月,P<0.0001),但 OS 无显著差异(8 vs 7.2 月,P=0.094)。接受酪氨酸激酶抑制剂(TKI)联合 ICI 治疗的患者的 PFS 和 OS 分别为 6.4 和 18.9 月,看起来比单独使用 TKI 更好。该研究还发现,接受 T+A 治疗期间 PFS 较短的患者,二线治疗的 PFS 也更短,这提示这些患者的肿瘤可能恶性程度更高,前线治疗效果不好,后线治疗疗效往往也不好。
ABSK-011 用于 FGF19-FGFR4 通路激活的肝癌二线治疗的 I 期研究(1012P)
大约 30% 的肝癌患者存在这个通路的异常激活,ABSK-011 是上海和誉的一个靶向 FGFR4 的抑制剂。在这项 I 期研究中,除了确定推荐的 II 期研究剂量,还要初步评估治疗的疗效。研究一共入组了 FGF19 高表达的肝癌患者 72 例,这些患者至少接受过一线系统治疗。疗效方面,在可评估的 65 例患者中,包括了每日 1 次用药和 2 次用药的患者,RECIST v1.1 评估的 ORR 20%。而在接受每日 2 次用药的 23 例患者中,ORR 达到了 43.5%。治疗较为安全,≥3 级的 TRAE 发生率 29.3%。在经治的肝癌患者中获得这些疗效数据,这个药物还是很挺让人期待的。
HCC 的围手术期治疗
肝动脉灌注化疗(HAIC)联合多纳非尼和信迪利单抗用于不可切除肝癌转化治疗的 II 期研究(DoHAICs)(999P)
这项 II 期研究一共入组了 30 例受试者,其中 BCLC A、B、C 期患者分别为 4、10、16 例。中位肿瘤直径 7.9 cm,近一半的患者伴有大血管癌栓。疗效方面,根据 mRECIST 标准,ORR 82.1%,其中 4 例 CR,19 例 PR。13 例(43.3%)患者在治疗后接受了手术切除,5 例病理学完全缓解。整体而言,这项联合治疗方案作为转化治疗,显示出了可靠的疗效。
仑伐替尼联合信迪利单抗用于不可切除肝癌的转化治疗的 II 期研究(946P)
这项研究入组了 137 例不可切除肝癌患者,其中 100 例仅接受了药物治疗且存在评价信息纳入了最终分析。这 100 例患者中,58 例伴有门静脉癌栓,4 例伴有下腔静脉癌栓,7 例两者皆有。26 例伴有肝外转移。在术前的影像学评估中,mRECIST 评估的 ORR 和 DCR 分别为 54% 和 77%。最终有 47% 的患者接受了手术切除。在中位随访 17 月后,中位 OS 25 月,其中接受手术的患者的中位 OS 未达到,未能接受手术的患者中位 OS 15 月。接受手术的患者中位 RFS 为 25 月。 因为入组的患者基线不同,很难比较不同方案的转化切除效率。但无论如何,系统治疗联合或不联合局部治疗都可以让一部分初始不可切除的肝癌患者获得手术切除的机会,并且术后疗效看起来都不错。
HAIC 联合安罗替尼和 TQB2450 用于肝癌术后辅助治疗的单臂探索性研究(951P)
TQB2450 是正大天晴的 PD-L1 抑制剂。研究入组了 72 例伴有高危复发因素的肝癌患者,术后接受两个周期的 HAIC 治疗,同时接受 4 或 8 个周期的安罗替尼口服联合 TQB2450 用药 4 个周期。这些患者者 67.7% 伴有微血管侵犯,33.8% 肿瘤直径≥8cm,7.4% 有≥3 枚病灶。在中位随访半年后,仅 1 例出现了肿瘤复发,1 年的 DFS 率 85.7%。从这项单臂研究看,疗效数据还不错。
胆管系统肿瘤(BTC)
度伐利尤单抗单抗联合化疗用于 BTC 一线治疗的中国区扩展队列数据(98P)
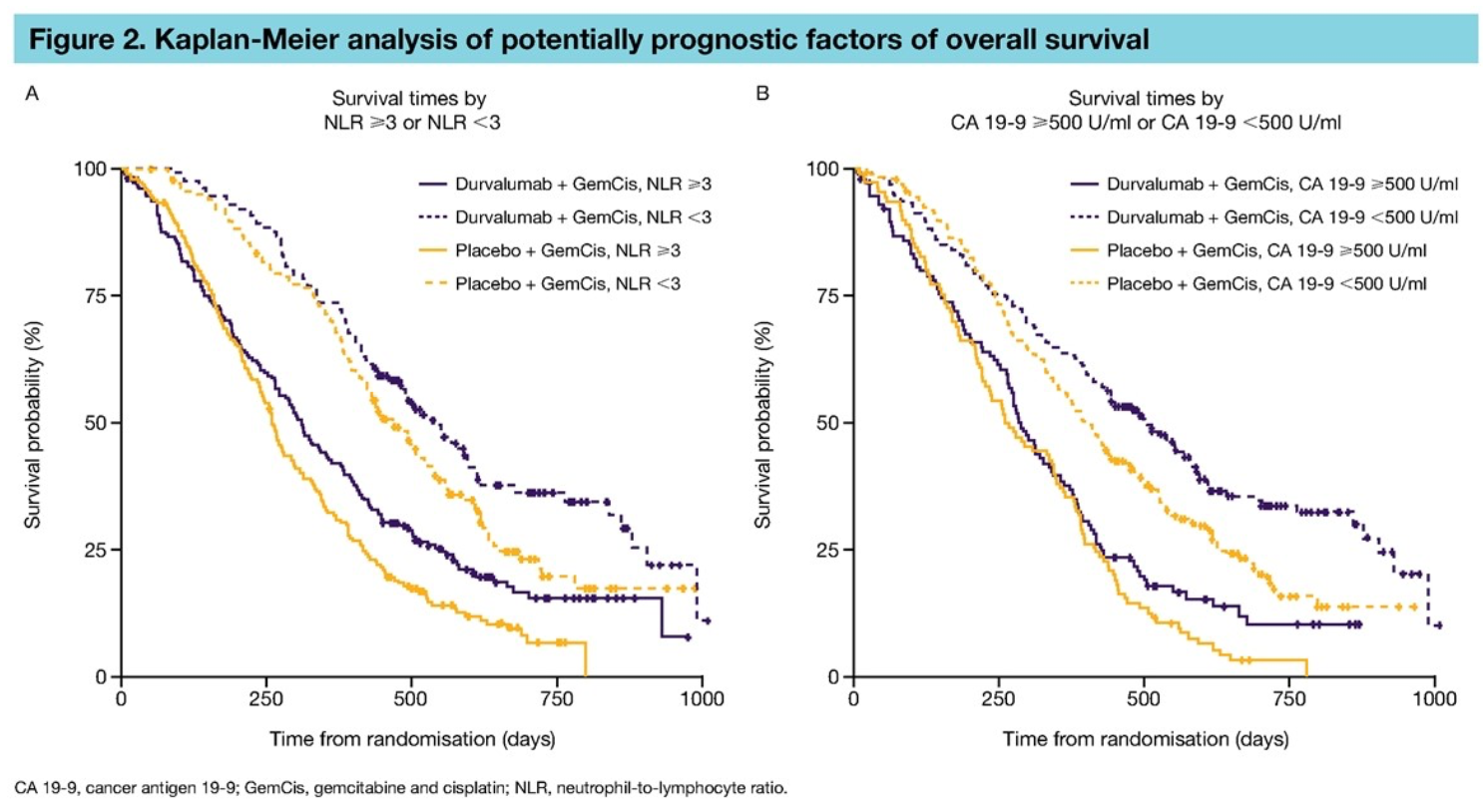
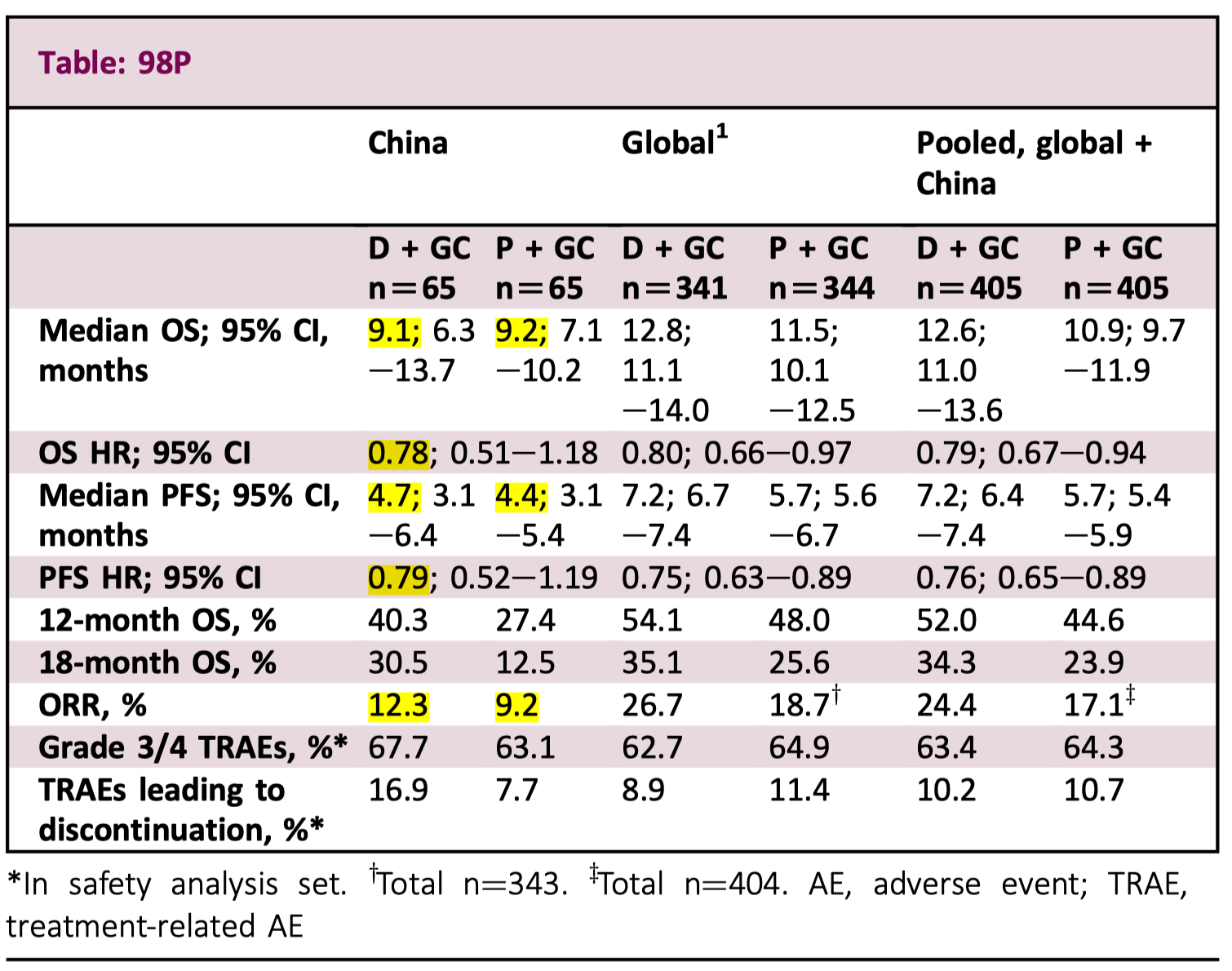
TOPAZ-1 研究发现在吉西他滨联合顺铂(GC 方案)的基础上增加度伐利尤单抗,可以进一步改善胆管癌患者的 OS 和 PFS,从而让该方案成为了不可切除晚期胆管癌的标准一线治疗方案之一(另一个方案是帕博利珠单抗联合 GC 化疗)。但 TOPAZ-1 研究在中国大陆地区入组只入组了个位数的患者。应监管要求,增加了中国扩展队列。这样一来,在大陆地区总共入组了 130 例受试者。与全球结果一致,与安慰剂联合化疗相比,度伐利尤单抗联合化疗可以改善患者的 OS 和 PFS,因为入组的样本量相对较小,没有达到统计学差异,这些结果都不奇怪。但是我们却注意到,中国区的患者 OS、PFS 和 ORR 均比全球患者差不少(下表)。从公布的基线数据看,国内入组的患者基线情况差一些,例如国内患者中 PS=1 分占 70% 左右,而全球人群中 PS=1 分只占一半左右。 此外,今年同样还有一项研究分析了 TOPAZ-1 研究中与预后相关的因素(102P),其中 PS=1 分(相对于 0 分)与不良预后显著相关(HR=1.29),此外,NLR≥3,CA19-9≥500U/mL 也是与不良预后相关的因素,HR 分别为 2.14 和 2.08。
SHR-1316(阿得贝利单抗)联合 IBI310 用于肝内胆管癌的二线治疗的 II 期研究(105P)
胆管癌在含吉西他滨进展后的二线治疗选择非常有限,目前的标准二线治疗是 FOLFOX 方案化疗,但患者的获益很少。这项 II 期研究入组了 39 例肝内胆管癌患者,他们都接受过化疗,其中分别有 21 例和 26 例还接受过 PD-1 抗体免疫治疗和小分子靶向药物治疗。SHR-1316(阿得贝利单抗)是恒瑞的 PD-L1 抗体,IBI310 则是信达公司的 CTLA-4 抗体。在目前可评价的 25 例患者中,2 例出现了完全缓解,3 例部分缓解,ORR 和 DCR 分别为 20% 和 60%。并且,在 13 例 PD-1 抗体经治的患者中有 2 例患者缓解。≥3 级 AE 发生率为 41%。看起来,这种采用两个免疫检查点抑制剂的方案还是可以使部分后线治疗患者获益。
Tinengotinib 用于抗 FGFR 治疗治疗耐药的胆管癌的初步数据(95MO)
Tinengotinib 是南京药捷安康开发的一个强效 FGFR2 抑制剂。这项研究一共入组了 73 例晚期胆管癌患者,其中 47% 曾接受过抗 FGFR 治疗。安全性方面,G3/4 TRAE 发生率 47.9%,最主要的 TRAE 是高血压、口腔炎、腹泻和手足皮肤反应(这些不良反应跟泛靶点的 TKI 倒是比较相似)。其中 58 例可以评估,ORR 20.7%,DCR 75.9%。在 29 例接受过抗 FGFR 治疗的 FGFR2 变异的患者中,ORR 34%,DCR 89.7%。21 例前期 FGFR 抑制剂治疗后出现获得性耐药的患者中,ORR 38.1%,DCR 95.2%。这些结果显示这个新药的抗肿瘤活性不错,值得进一步探索。
贝伐珠单抗联合厄罗替尼用于化疗有效的患者的维持治疗的随机对照研究(BEER-BTC)(99P)
这是一项 II-III 期临床试验,目前报道的是 II 期部分的结果。研究在印度开展,入组的是接受了含有吉西他滨的治疗并且在治疗 6 月后肿瘤缓解或者疾病稳定的患者,按照 1:1 的比例接受贝伐珠单抗联合厄罗替尼维持治疗或停药监测。目前入组了 98 例受试者,结果显示,接受维持治疗的患者 PFS 更长(5.2 月 vs 3 月,P=004),并且没有 3 级以上不良事件发生。目前 III 期研究已经在开展,需要对比两组的 OS。 目前 BTC 的一线治疗已经发生改变。以往,在吉西他滨联合铂类化疗 6-8 周期后,就可以选择停药观察,但现在需要使用免疫治疗作为延续的维持治疗。而在东方的临床实践中,GC 化疗在铂类累积剂量达到之后,往往还会有吉西他滨的单药维持治疗。因此,这项研究可能需要修改干预方案,至少需要探索免疫治疗联合这两个靶向药物 vs 免疫治疗作为维持治疗的疗效。
肝外胆管癌术后辅助治疗(GC vs 卡培他滨) II 期研究的最终分析结果(STAMP)(104P)
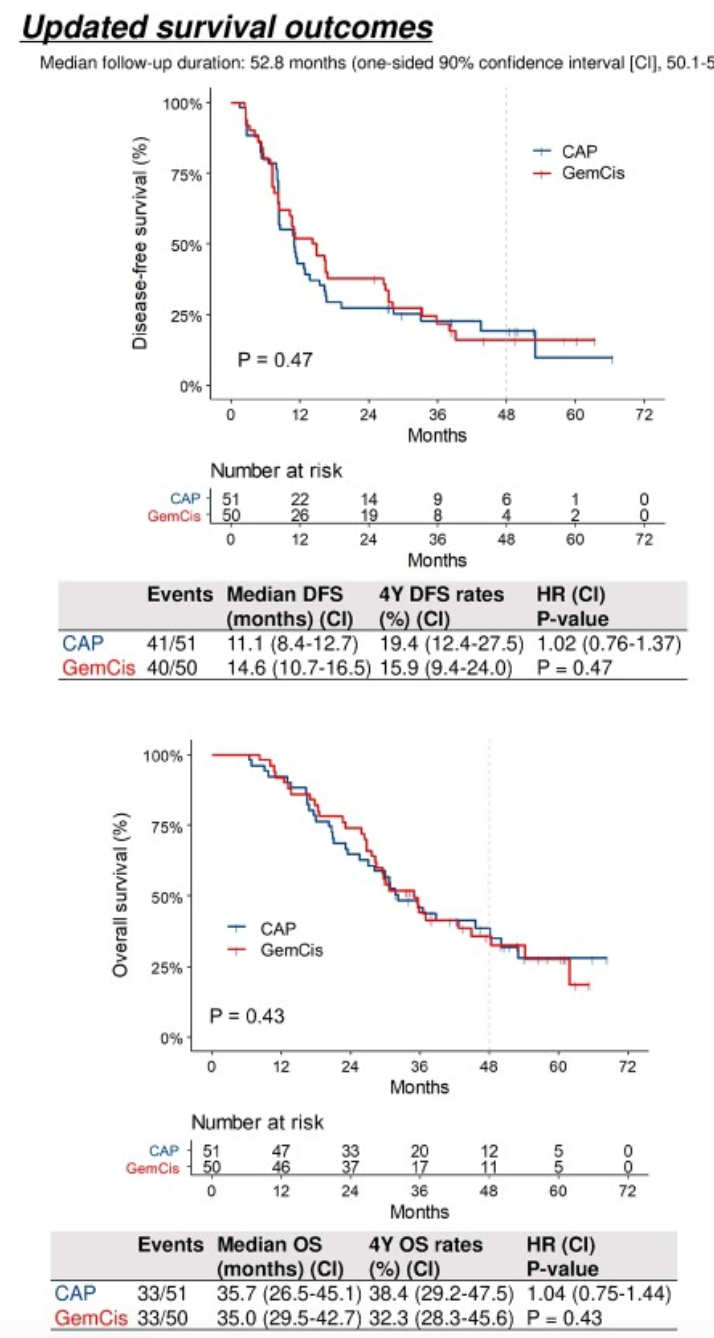
目前,卡培他滨是合并高危复发因素的胆管癌患者的术后辅助标准治疗,替吉奥也可以作为替代。理论上讲,对于复发风险更高的患者,使用更高强度的辅助治疗可能会疗效更好。STAMP 是一项在韩国开展的随机对照的 II 期研究,这项研究入组的是合并区域淋巴结转移的肝门胆管癌和远端胆管癌患者。101 例患者按照 1:1 的比例随机接受 GC 方案静脉化疗或卡培他滨口服化疗。前期已经报道过,GC 化疗并没有改善患者的 DFS(14.6 月 vs 11.1 月,HR=1.02,P=0.47),4 年 DFS 也相似,分别为 15.9% 和 19.4%。这次报道了成熟的 OS 结果,两组同样没有差异(35.0 vs 32.3 月,HR=1.04,P=0.43),4 年 OS 分别为 35.7% 和 38.4%。由此可见,与卡培他滨相比,即使增加了化疗的强度,并没有更好推迟肿瘤复发或延长患者生存。
度伐利尤单抗联合 GC 化疗用于局限期胆管癌新辅助化疗的随机对照 II 期研究(DEBATE)(97P)
在这项随机对照的 II 期研究中,局限期的胆管癌患者按照 2:1 的比例随机接受 4 个周期度伐利尤单抗联合 GC 化疗或单独化疗作为新辅助治疗。研究共入组了 45 例患者,其中 40% 是肝内胆管癌,69% 临床 III 期。术前治疗反应方面,两组的 ORR 分别为 36% 和 7%。分别有 68% 和 36% 的患者有机会接受手术探查,而分别有 61% 和 36% 的患者接受了 R0 或 R1 切除。两组的中位 PFS 分别为 15.1 月和 3.6 月。整体而言,如果入组的是初始可以切除的患者,这手术切除率有些偏低。化疗联合免疫治疗的有效率还没有足够高,可能还不能成为合格的新辅助治疗。因为研究没有设置直接手术的对照组,所以单独使用化疗或者化疗联合免疫治疗作为新辅助治疗会不会对患者有害,目前也不能确定。
