这期 JCO 杂志上又发表了一篇肠癌肝转移的研究。这是一项多中心的 III 期研究,评估的是在经过了一线的奥沙利铂或伊立替康为主的化疗失败的患者中,比较患者在接受二线化疗的同时,增加 Y90-微球经肝动脉放疗栓塞(TARE)治疗的疗效(EPOCH 研究)。
研究在北美、欧洲和亚洲国家开展,一共入组了428 例受试者,这些患者均不存在肝脏以外其他部位的转移灶。这些患者按照 1:1 的比例随机接受二线化疗+ TARE 治疗或单独使用二线化疗。
主要终点方面,两组患者的中位 PFS 分别为 8.0 月和 7.2 月(HR=0.69,95% CI 0.54-0.88,单边 P=0.00143));另一个主要终点是肝内病灶的 PFS(hPFS),两组分别为 9.1 和 7.2 月(HR=0.59,95% CI 0.46-0.77,单边 P<0.0001)。
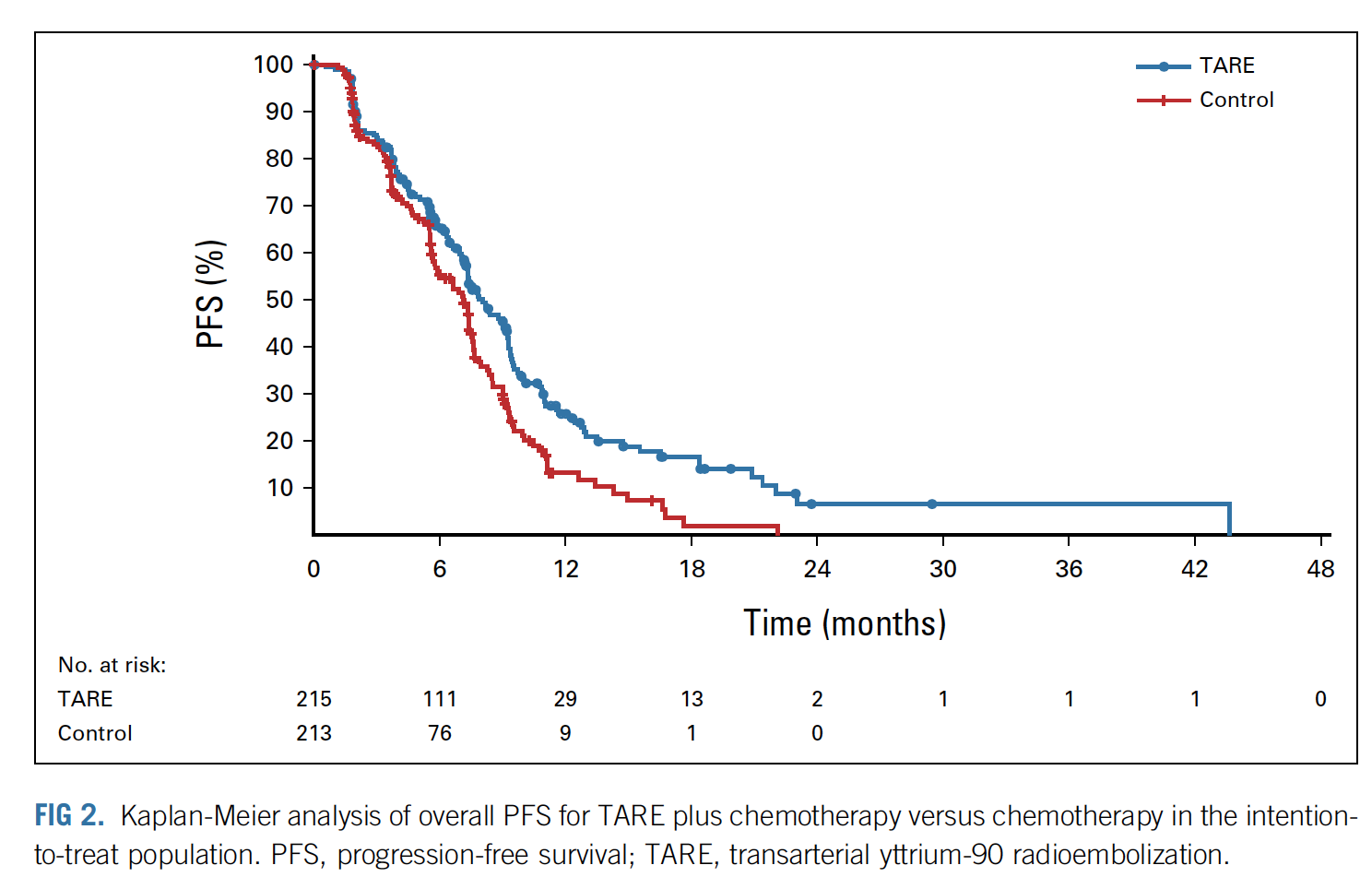
次要终点方面,两组的 ORR 分别为 34% 和 21.1%(P=0.0019),然而,两组之间的总体生存却没有统计学差异。整体而言,患者在一线治疗进展后,生存时间 1 年左右,两组的中位 OS 分别为 14.0 月和 14.4 月(HR=1.07,95% CI 0.86-1.32,P=0.7229)。如果按照 per- protocol 的方式分析,TRAE 组的中位 OS 在数值上有微弱的优势(15.2 月 vs 14.3 月,HR=0.96,单边 P=0.3841)。
安全性方面,增加了 TARE 带来了更多的 AE,两组的 3 级及以上 AE 的发生率分别为 68.4% 和 49.3%。
尽管研究者庆祝了这项研究在两个主要研究终点上取得了阳性结果,但 TARE 这样的针对肝内病灶的治疗是否值得向患者推荐值得进一步讨论。这项研究的结果跟近期的肝转移灶 R0 切除后的辅助治疗的研究有些相似。这两项研究都在替代终点(PFS 或 DFS)上出现了阳性结果,但在 OS 上却是阴性结果。那这样的治疗措施(TARE 治疗或者根治性手术后的辅助化疗)在临床上是不是值得推广呢?个人的态度是,还是需要谨慎推荐这些治疗,因为这些治疗会增加了不良事件的发生率。如果 OS 没有差异,需要证明这些治疗在改善替代终点的同时改善了患者的生活质量,否则这样的治疗就是有害的。所以,这些研究都需要报道患者报告的终点,如果能够证明这些治疗在推迟肿瘤进展或推迟肿瘤复发的同时,可以改善患者生活质量或者推迟患者生活质量的恶化,那这样的治疗才值得临床应用。
