
2008 年发表在 JNCI 杂志上的 “Design and endpoints of clinical trials in hepatocellular carcinoma" 一文是我在肝癌临床研究领域的启蒙读物。近期 Llovet 教授等更新了这篇纲领性的文章,我精读了一遍,把读书笔记贴在这儿。
不同分期的肝癌病人,预期生存期分别是:A期,5年;B期,20-30月;C期,10-16月。
最近15年没有什么太大成就的领域:筛查和早期发现肝癌;切除或消融后的辅助治疗;中期肝癌的治疗。
优秀的临床试验除了考虑PICO原则,还需要预先设定数据分析计划(data analysis plan)。
如果使用modified Jadad score来评价,2002-2005年间的报道的肝癌临床研究只有一半左右质量较高。
相比较FDA审批药物,指南的要求可能更高。FDA可能会基于ORR这样的替代终点审批药物,但指南需要考虑的更高的证据等级。
研究终点方面
终点事件分3种:硬终点(hard),替代终点(surrogate)和病人报告的终点(patient-reported endpoint)。病人报告的终点有时也叫做软终点。
FDA使用替代终点来加速审批药物本来是在HIV流行的最艰难的时期用来快速审批抗病毒药物的。
非劣效设计的临床试验,HR=1.08是FDA认可的95%置信区间的上限。
不同的进展类型也影响进展后生存,出现新的肝外病灶和/或血管侵犯的病人生存期较短,而原有病灶的长大或肝内出现新病灶的病人,则生存期相对较长。
因为目前的现状是,TACE进展后的病人有60%接受了后续治疗,一线全身治疗失败的病人有50%接受了后线治疗,所以PFS可以作为可以替代的终点。
在肝癌的21个RCT中,PFS与OS的相关性比较一般,PFS方面的HR<0.6则可以用来预测OS方面获得阳性结果(下图,我增加了近期的3个研究的数据)。
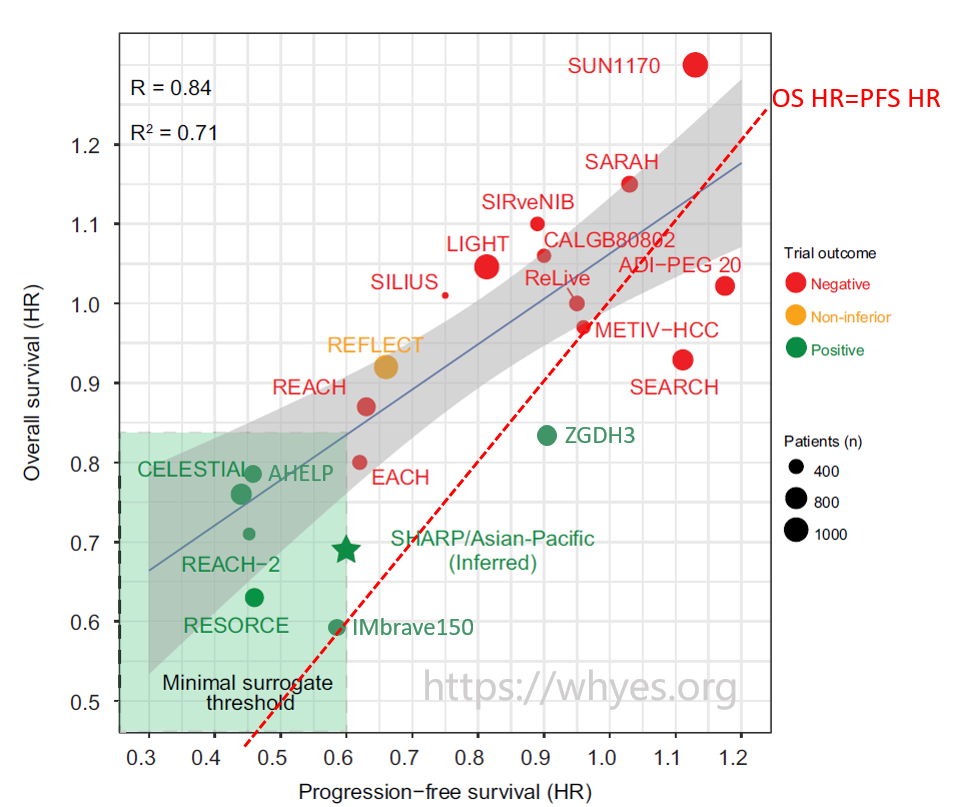
目前失败的临床试验来看,一些在别的肿瘤有效的新药,对肝癌病人而言,毒性太大了。
DoR在ICI治疗时大约是12月,而TKI治疗时则不到6个月。
筛查和化学预防
尽管我们已经有慢性乙肝或者慢性丙肝患者肝癌发病率的数据,但是目前没有接受了丙肝根治、抗病毒药物治疗后的乙肝病人,还有NAFLD病人的确切数据。
对于化学预防的药物,3级以上的不良事件是不可接受的,而对于肝癌的治疗而言,30-50%的3、4级不良事件是可以接受的。
肿瘤早筛需要符合NCI Early Detection Research Network (ERRN)制定的5-phase program。
早期肝癌
目前是有一些比较高质量的随机对照研究发现某项辅助治疗可能有效的,但是都没有被重复出来。
AASLD还是坚持认为不应大扩大手术切除的适应证,然后再来研究辅助或新辅助治疗。
作者认为,AASLD和EASL指南只认临床证据,而亚洲指南加入了专家共识和临床实践的经验。亚洲指南将多发肿瘤和癌栓病人纳入了手术切除的指征,因此在设计辅助治疗临床试验时,需要将这些因素加入考虑,作为分层因素。
新辅助治疗之前的活检是必须的,通过对比手术前后的标本,可以更好地研究肿瘤免疫微环境。
新辅助治疗,可以选择病理学缓解率和1年复发率作为研究终点。
符合米兰标准的肝癌肝移植术后的肿瘤复发率相对较低,10-20%。
AASLD和EASL指南认为2cm以下的肿瘤消融治疗首选,超过这个界值,手术切除首选。
ALBI比Child-Pugh分级对肝功能的评估会更加客观。
还有个HAP score,包括胆红素、白蛋白、肿瘤大小和AFP。
中期肝癌
对于中期病人而言,系统治疗不仅可以作为TACE的后续治疗,甚至还可以评价是否可以成为TACE的替代。对于超过up-to-seven标准的病人,尤其应该探索系统治疗的优势。
晚期肝癌及药物治疗
RECIST 1.1和mRECIST相比,在评估肿瘤进展相关的终点时,例如PFS和TTP,基本相似。
使用影像学来评价ICI的治疗反应,8-12周的这种更长间隔比较合适(排除治疗早期的假性进展),而评价TKI,使用6-8周更合适。
REFLECT研究排除了门脉主干癌栓、肿瘤累及50%以上肝脏、胆道癌栓的病人,所以对这部分病人,索拉非尼和仑伐替尼之间的差别未知。
索拉非尼-瑞戈非尼序贯治疗可以达到26月的生存期,这个数据不靠谱,因为这些病人首先得有机会接受二线治疗。
单臂的II期研究来评价某个TKI的疗效,ORR超过20-30%的话,更有可能在后期的研究中赢出。
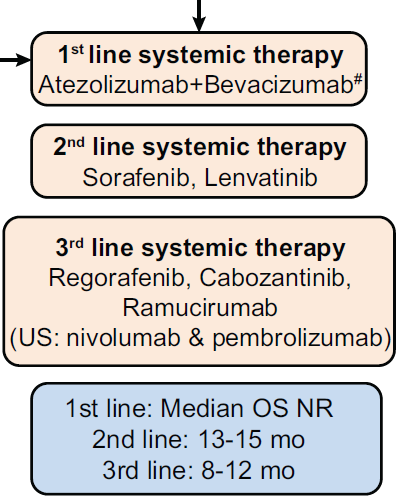
T+A组合获批之后,原有的一线治疗,包括索拉非尼和仑伐替尼将会移至二线治疗。
对于免疫治疗,ORR与OS的相关性不好,有作者推荐使用6月-PFS率来作为2期研究的终点。
作者畅想,系统治疗在不远的将来,将会用于肝癌各个分期的治疗,与现有方式的结合(手术前后的新辅助、辅助治疗;TACE进展后治疗或与TACE联合,或替代TACE)。
某些临床试验是 statistically negative but "clinically positive",说的是KEYNOTE 240研究。如何认定clinically meaningful benefit,一般认为OS方面的HR<0.8。事实上,所有阳性的研究的OS方面的HR都小于0.8。
分子分型/生物标志物
基于分子分型/生物标志物的研究还是有的,例如失败的tivantinib基于MET高表达的病人;REACH-2研究,雷莫芦单抗用于AFP>400的病人;另外还有FGFR-4抑制剂用于FGF-19高表达的病人,ORR是16%。在肝癌做到这点有很大困难,因为实践上肝癌不需要借助活检就可以无创诊断,最常见的驱动突变都不能干预;只有25%的肝癌病人有可干预的变异。
作者鼓励做更多的穿刺活检和高敏感性的液体活检,这被成为肝癌治疗的 cultural change 。
CTNNB1-mutated HCCs are immune excluded and potentially resistant to immune checkpoint inhibitors.
生活质量
FDA要求使用PRO-CTCAE来报告病人的生活质量。"symptomatic side effects"
SHARP研究中,其实有两个主要终点:病人的生存率方面,索拉非尼优于安慰剂,但在time-to-symptomatic progression方面,索拉非尼比安慰剂还差一些(下图)。
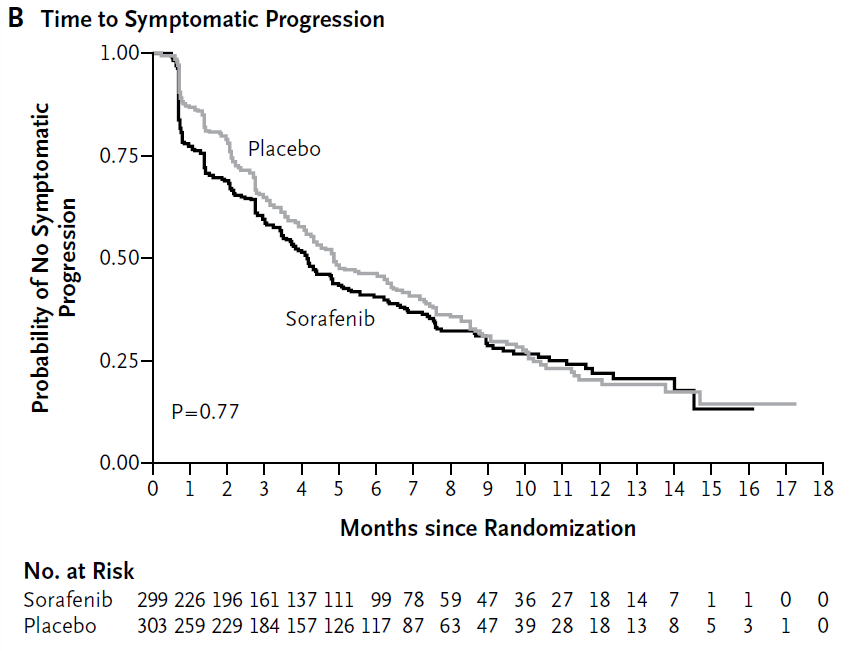
Ref: Llovet JM, et al: Trial Design and Endpoints in hepatocellular carcinoma: AASLD Consensus Conference. Hepatology, 2020, doi: 10.1002/hep.31327