今年 ASCO 全体会议上的同场评论“From Insight to Impact: Driving Plenary Knowledge into Action This Monday”,令我深有共鸣,直译成中文是:将全体会议上获得的知识化转化为下周一的临床实践。在回顾今年肝细胞癌的临床研究进展之后,我们有必要回归实践,审视这些发现将如何改变我们的治疗决策。

可切除肝癌
中国肝癌分期(CNLC)Ia-IIa 期的患者,指南推荐首选手术切除,但其中 Ib-IIa 期的患者,肿瘤较大或者肿瘤多发,手术后的复发风险比较高。以往,我们会先做手术切除,手术后再辅以预防性的经肝动脉化疗栓塞(TACE),部分中心也在尝试使用药物治疗来预防复发。但药物作为术后辅助治疗缺少高级别证据。目前多项回顾性研究提示,术后辅助免疫治疗可预防复发,但回顾性研究本身的偏倚无法克服。辅助治疗有效性的问题,还需要前瞻性的对照研究来回答。
术后辅助治疗
去年的 ESMO 会议上,IMbrave050 研究(肝癌术后辅助治疗:阿替利珠单抗+贝伐珠单抗 vs 主动监测)更新了随访结果。该研究显示,阿替利珠单抗联合贝伐珠单抗(T+A 方案)辅助治疗不能改善 RFS,也不能改善 OS。晚期肝癌的优选治疗方案用于术后辅助治疗并没有出现意想的降低肿瘤复发的效果,这有些违背直觉,但我们不得不接受这个的现实。
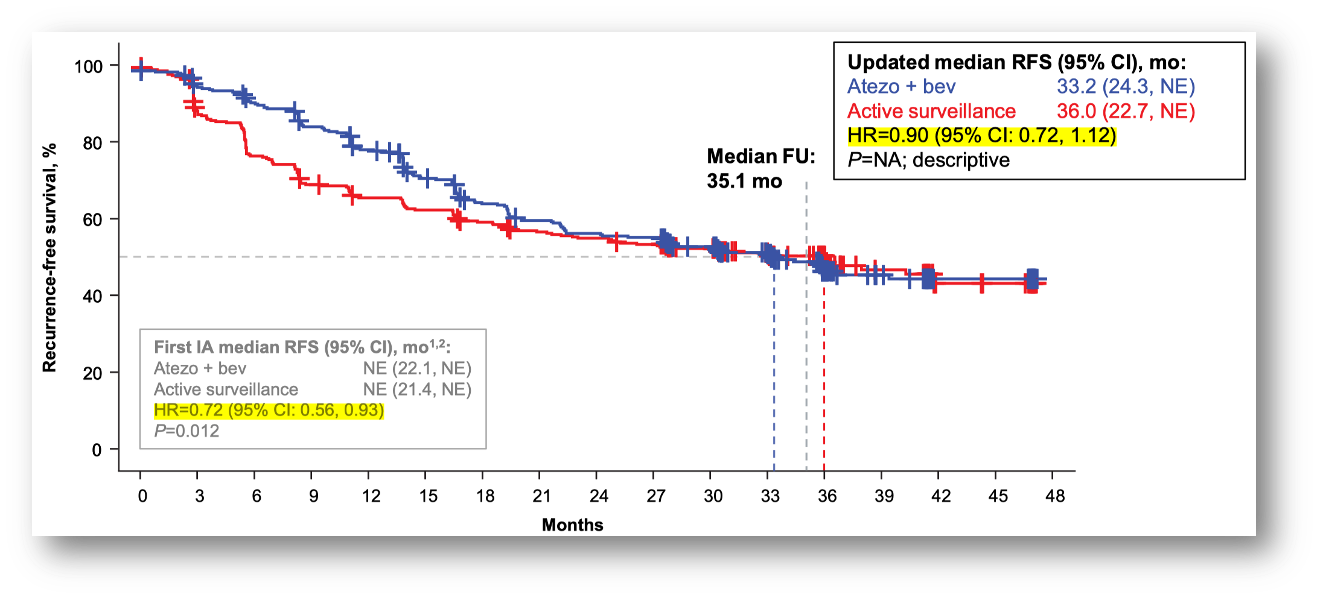
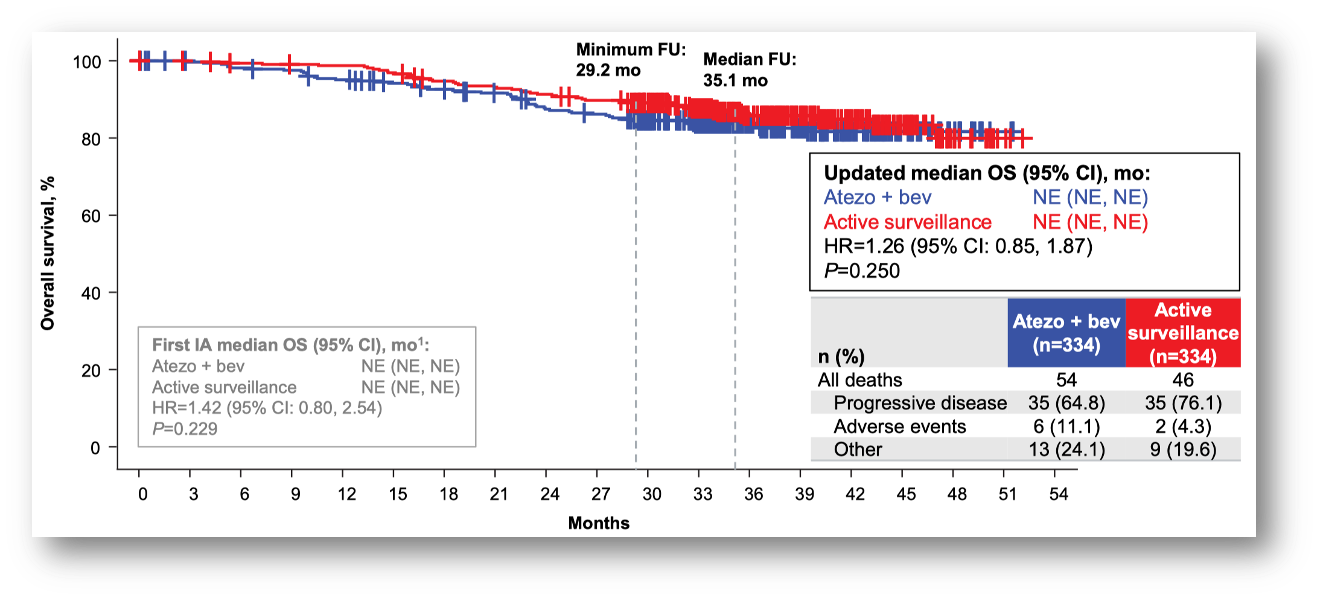
2025 年 7 月,KEYNOTE-937 研究(肝癌术后辅助治疗:帕博利珠单抗 vs 安慰剂)的申办方通知研究者,帕博利珠单抗辅助治疗也不能降低术后复发,该研究没能达到主要研究终点。这项研究预设的无复发生存期(RFS)的 HR 值是 0.7(即肿瘤复发风险下降 30%),现在的悬念是 PD-1 抗体到底能将肝癌术后的复发风险下降多少,我推测最终的 HR 可能在 0.90-0.95 之间,期待在即将到来的 ASCO GI 2026 会议上这项研究公布的结果。

但是,这项阴性结果的临床研究却可能会改变国内的临床实践。尽管缺少确切证据,在国内,靶向或免疫治疗被用于肝癌术后辅助治疗比较广泛,现在已经有两项研究明确提示了术后免疫治疗或靶向联合免疫治疗都是无效的,不知道国内的术后辅助治疗的应用能不能减少些。在 PubMed 上检索了肝癌术后免疫治疗回顾性研究,检索出来的 5 项研究无一例外都提示术后辅助免疫治疗可以降低肝癌复发。这提示,辅助治疗领域的回顾性研究存在很大偏倚,以至于跟前瞻性的研究出现了相反的结果。
至此,药物用于肝癌术后辅助治疗的几项大型研究均宣告失败,术后使用靶向治疗(索拉非尼,STORM 研究)、免疫治疗(帕博利珠单抗)、或靶向联合免疫治疗(T+A 方案)均不能降低复发。基于这些证据,除非是患者接受的是非根治性的手术,否则术后使用药物作为辅助治疗的必要性都不大。
那中高危复发的肝癌患者只有先接受手术,手术后密切随访,被动等待?
新辅助/围手术期治疗
根据免疫治疗的作用机制,将免疫治疗提前至手术前使用,可能具有更大的优势。在主瘤存在时开始免疫治疗,可以诱发出更为多样和强效的免疫反应;手术切除后续贯用药,则可能有更好的免疫监视作用。今年的 ESMO 年会上,CARES-009 研究公布了无时间生存期(EFS)的结果。该研究入组了初始可手术切除 CNLC Ib-IIIa 期患者,术前接受 2 个周期的双艾组合(阿帕替尼+卡瑞利珠单抗)治疗,手术后续贯双艾治疗(围手术期治疗模式),最长1年时间;对照组则直接接受手术切除。结果显示,与直接手术相比,围手术期治疗显著改善了 EFS。通俗讲,术前+术后的围手术期治疗模式可以显著推迟肝癌术后复发。并且,CNLC Ib-IIa 期这些指南推荐首选手术切除的患者也从围手术期治疗中获益。
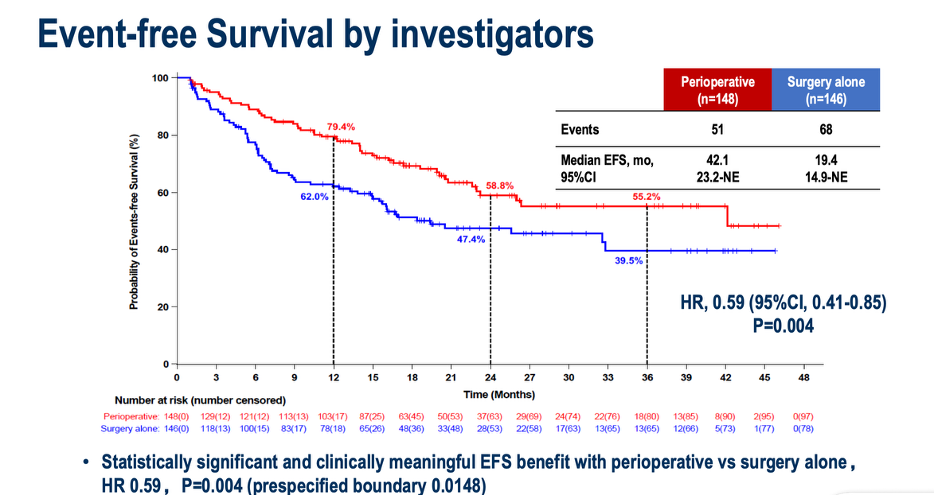
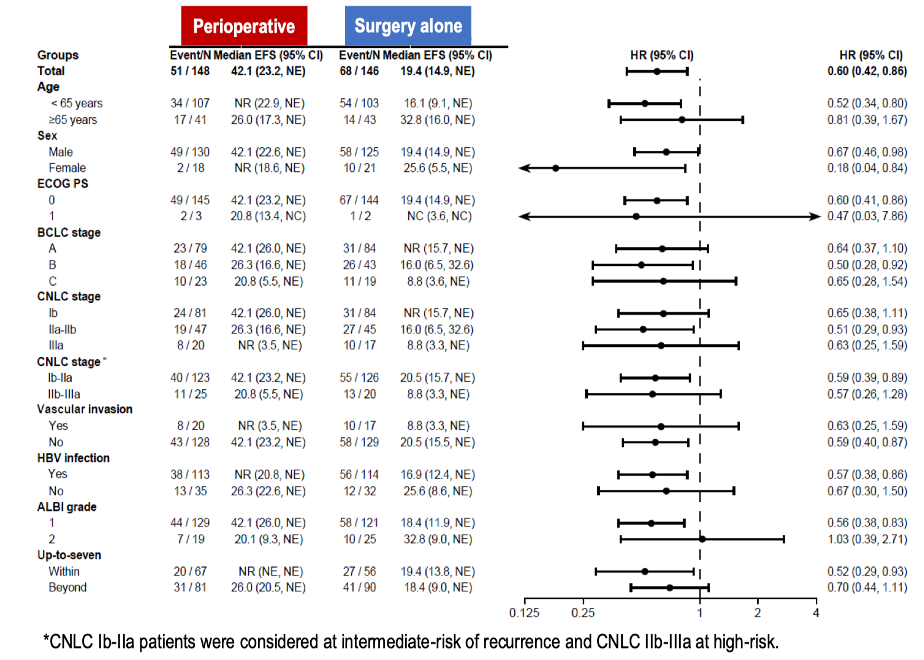
该研究是可切除肝癌治疗模式的革新,具有高危复发因素的可切除肝癌 可以考虑 推迟手术,先接受系统治疗作为术前的新辅助治疗。如果在进一步的随访中可以观察到 OS的改善(或改善趋势),该方案可成为这些患者的标准治疗手段。在临床实践中处理具体患者时,还要考虑新辅助治疗疗程的个体化,并可根据病理学反应结果确定术后续贯治疗的方案和疗程。
中期肝癌
一直以来,中期为主的肝癌(包括不可切除早期和门静脉远端分支癌栓的晚期肝癌)被认为是适合 TACE 治疗的人群,在 TACE 治疗无效之后,再接受系统治疗,这就是 中期肝癌传统的 TACE 续贯系统治疗模式。现在晚期肝癌的系统治疗取得了较大进步,如果在 TACE 治疗失败之前就开始使用系统治疗,可以形成 TACE 联合系统治疗的模式。联合治疗是否可以胜过续贯治疗,需要通过随机对照研究来评价。
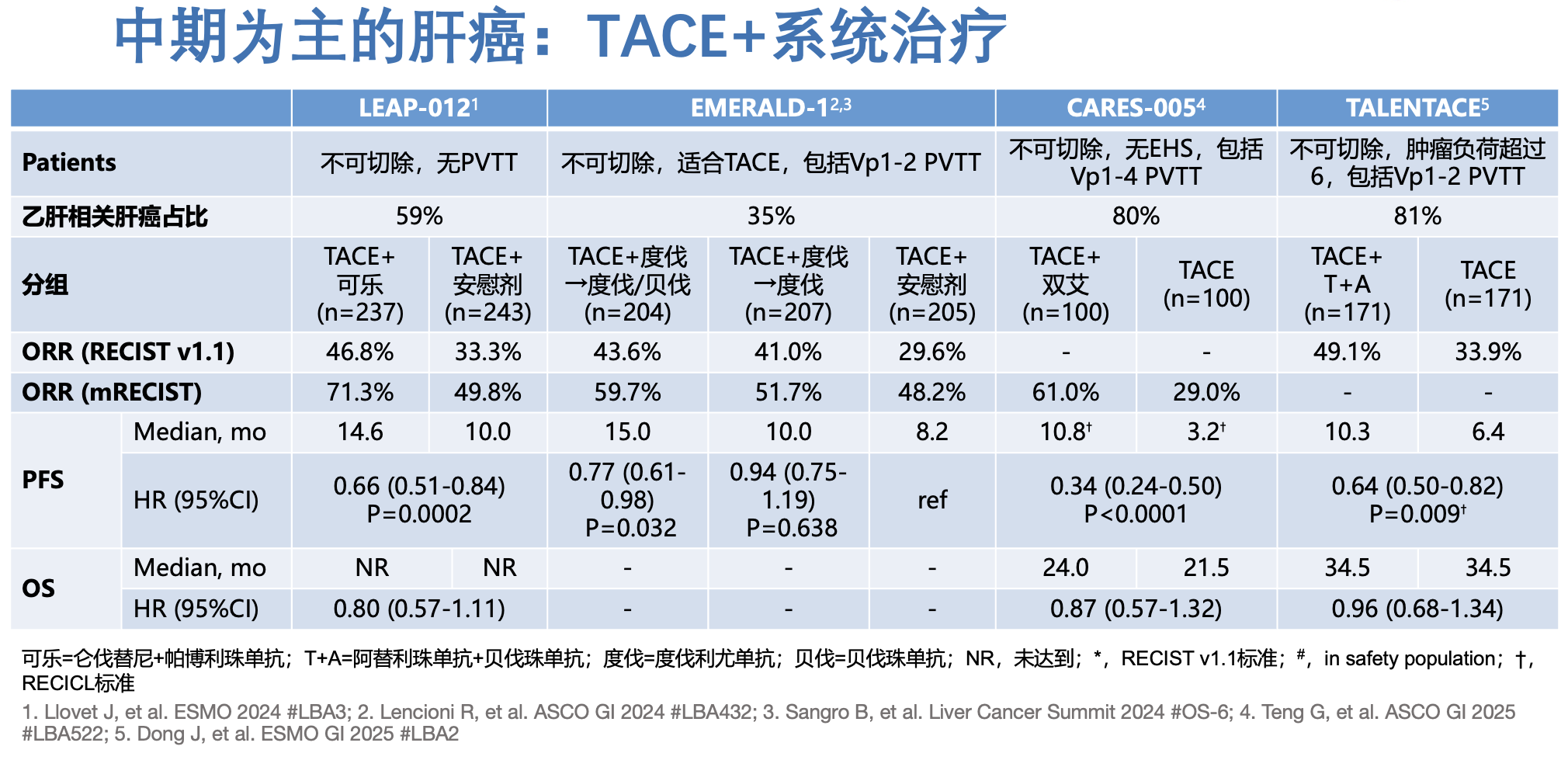
该领域已经有了 4 项随机对照研究公布了主要研究结果。这些研究使用的系统治疗方案不同、联合治疗的顺序有少许差异,但都提示在 TACE 治疗的基础上增加靶免治疗可以提高 ORR、显著改善 PFS。目前这些研究的 OS 数据都不成熟,但从已经公布的结果看,OS 的显著获益都难以达到。其中 LEAP-012 研究中 OS 的获益趋势最为明显,HR=0.80。但今年 10 月, 默沙东和卫材公司公告 该研究的 OS 期中分析未达到统计学差异,并且预期后续的 OS 分析也难以达到预设的统计学差异。这样一来,对于中期肝癌患者,系统治疗早用或者晚用对似乎对 OS 的影响不会太显著。那对于中期肝癌患者,TACE 等局部治疗还要跟系统治疗联用呢?个人认为,中期肝癌还需要进一步分层,首先根据患者的可手术切除状态进行分层,再根据肿瘤负荷确定治疗方案。
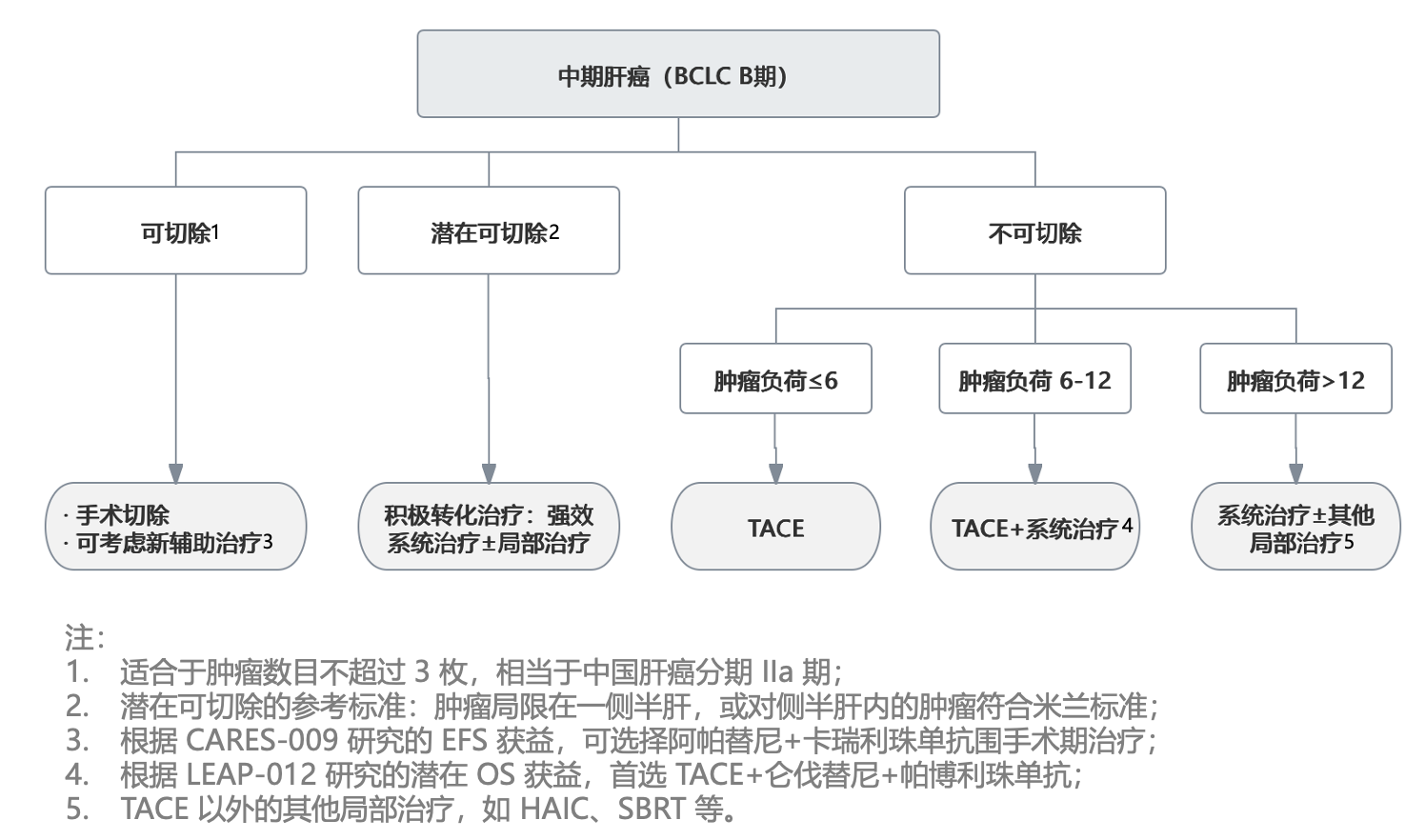
- 可切除。可切除的中期肝癌主要指的是肿瘤数目不超过 3 枚者(相当于 CNLC IIa 期)。但因为肿瘤多发,属于中高危复发风险,根据[[CARES-009]] 的 EFS 获益的结果,可考虑使用双艾组合新辅助治疗,手术之后再续贯使用。
- 潜在可切除。部分中期肝癌肿瘤数量不太多,或生长部位比较集中,在非手术治疗后有较大的几率转化成可手术切除的状态,这部分患者属于潜在可切除人群。潜在可切除标准目前没有统一。根据 一项回顾性研究 ,我们推荐肿瘤集中在一侧肝叶,或者对侧肝叶内存在肿瘤但对侧肝叶内肿瘤符合米兰标准者,作为潜在可切除肝癌。方案选择方面,可参考转化治疗共识,选择强效的系统治疗联合或不联合局部治疗。
- 不可切除。不可切除的患者需要根据肿瘤负荷进行分层,这里推荐使用 6-and-12 标准:
- 低肿瘤负荷者(≤6)对 TACE 治疗的获益较为确切,部分患者可以通过超选择 TACE 获得根治。这些患者首选 TACE 治疗,在 TACE 治疗不再获益后再考虑系统治疗,即继续应用 TACE 续贯系统治疗的模式。
- 中等肿瘤负荷者(6~12 之间)可考虑 TACE 联合系统治疗。LEAP-012 研究的亚组分析显示,这些患者接受 TACE 联合系统治疗后 OS 改善趋势明确,系统治疗方案首选仑伐替尼联合帕博利珠单抗(可乐组合)。
- 高肿瘤负荷者(>12)对 TACE 治疗的获益较少。在 EMERALD-1 研究根据肿瘤负荷的分层分析中 ,这样的患者接受 TACE 治疗 ORR 只有 3.6%,中位 PFS 4.8 月,而低负荷和中负荷的亚组的中位 PFS 分别为 11.1 和 9.7 月。这些患者宜选择 系统治疗作为一线治疗,在系统治疗的基础上可考虑增加 TACE 以外的其他局部治疗,如肝动脉灌注化疗(HAIC)、外放射治疗等。
晚期肝癌
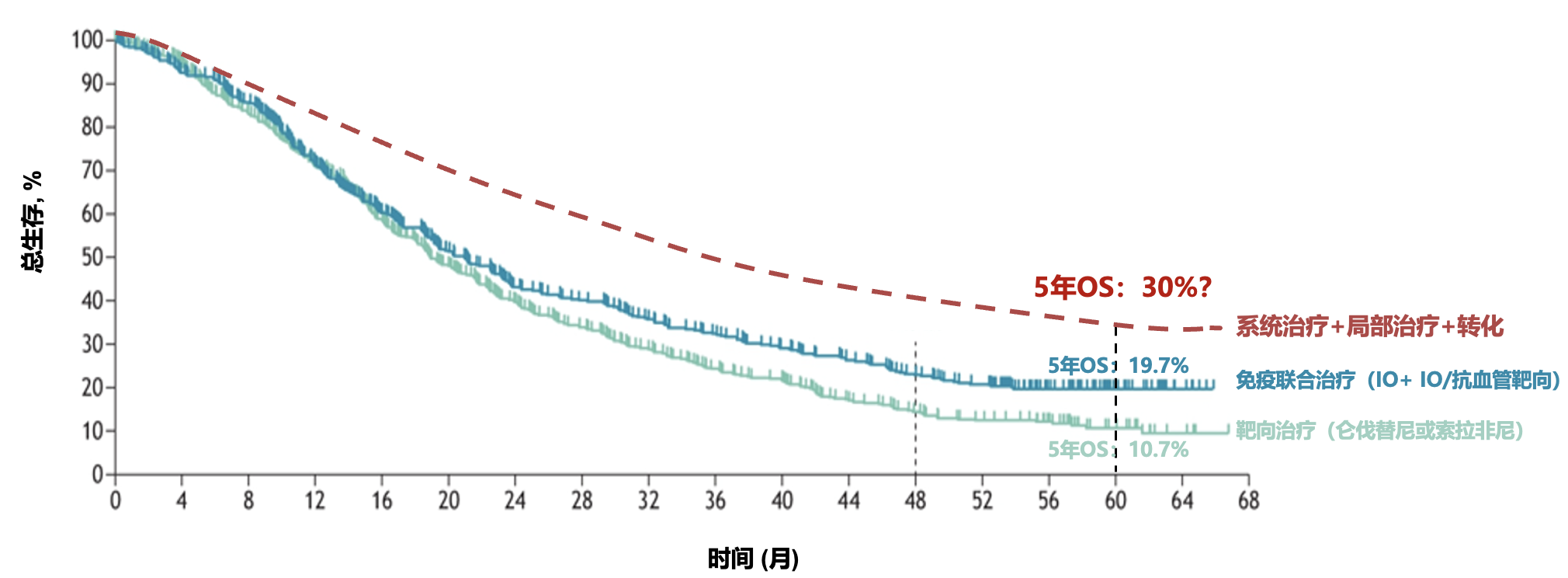
目前,不可切除或晚期肝癌的优选一线治疗方案都是免疫联合治疗,包括靶向联合免疫治疗和双免疫治疗。在免疫联合治疗时代,我们终于有机会讨论晚期肝癌的长期生存了。目前有两项 III 期研究公布了长期随访的结果,接受 STRIDE 方案(单次曲美木单抗+持续的度伐利尤单抗)双免疫治疗或可乐组合靶向联合免疫治疗的晚期肝癌患者的 5 年生存率都在 20% 左右。
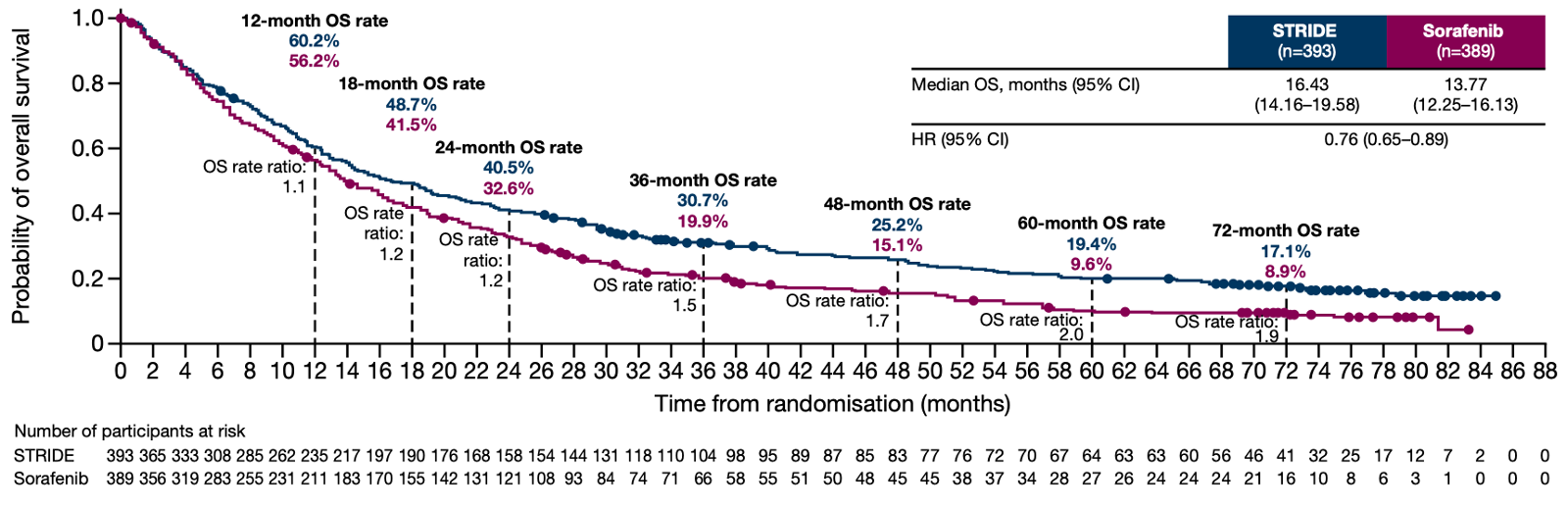
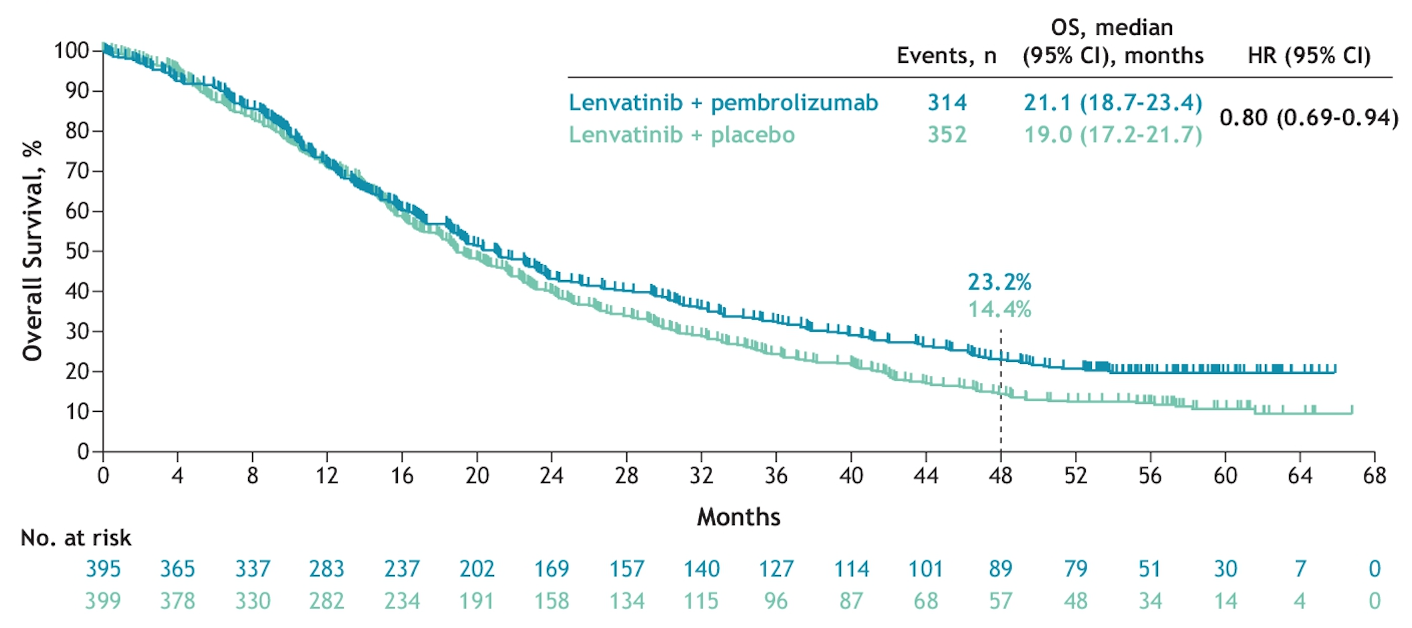
这些长期生存的患者可能大多是对免疫治疗获益的患者。为了进一步提高疗效,在现有治疗的基础上做加法可能是可行的方案。然而,今年 ESMO 会议上,有两项研究试图在现有标准一线治疗(T+A 方案)的基础上增加一种免疫治疗,但结果都不理想。
IMbrave152 研究中,在 T+A 基础上增加 TIGIT 抗体 tiragolumab 治疗,未能有效提高 ORR,也未能改善 PFS 和 OS。
研究者发起研究 TRIPLET HCC 显示,在 T+A 基础上增加小剂量 CTLA-4 抗体伊匹木单抗也没能进一步提高疗效。
如果没有更有效的药物出现,临床上灵活使用系统治疗和局部治疗手段可能为患者赢得更好的长期生存。在今年 ESMO 会议上,TALENTop 研究公布了主要研究结果。这项研究将接受 T+A 方案治疗 4 个周期后未出现肿瘤进展且可以手术切除晚期肝癌患者进行随机分组。治疗组接受手术切除,术后续贯使用 T+A 方案最长一年;对照组则接受 T+A 方案持续用药。研究显示,手术切除比持续系统治疗有更长的至治疗失败时间(TTF)获益,换句话说,手术切除延缓了患者一线接受 T+A 方案的失败时间,避免了患者出现治疗失败从而需要接受二线系统治疗;此外,OS 也显示出了改善的趋势。
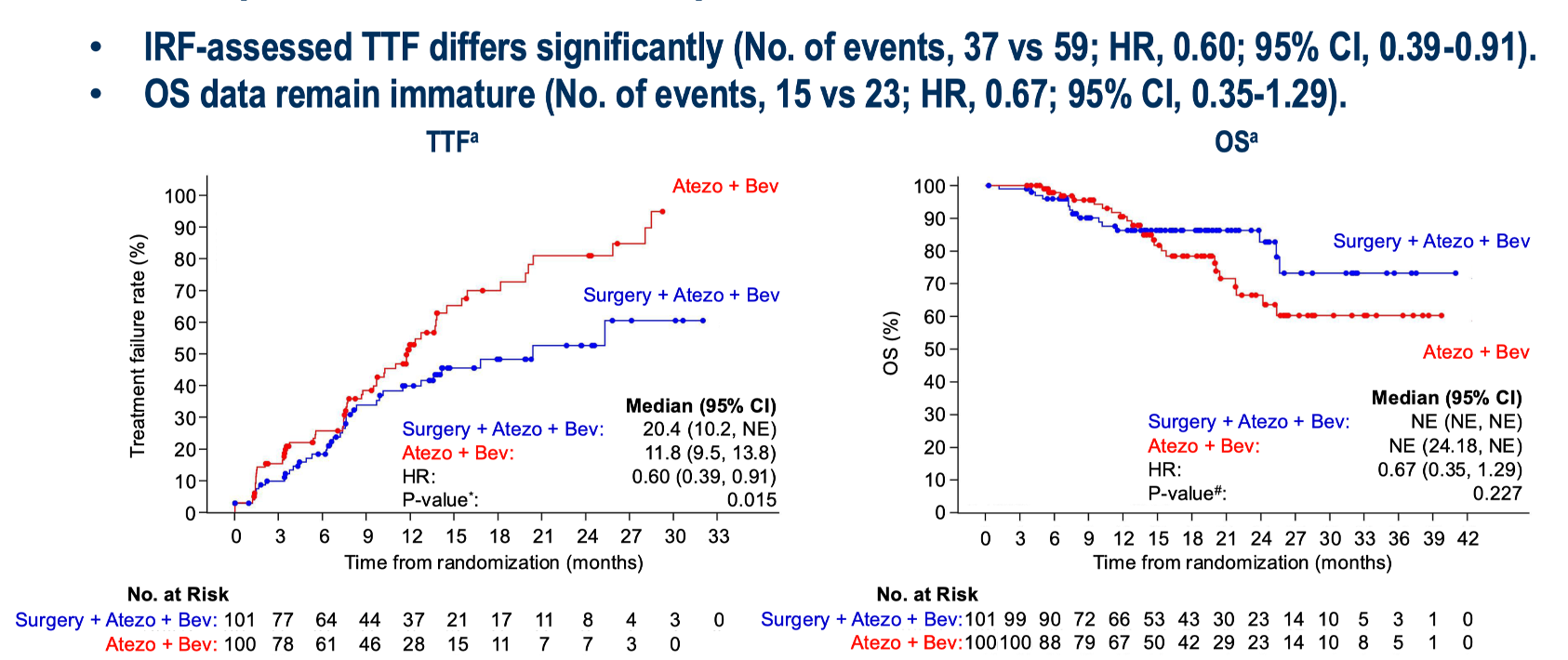
这项研究是首个通过前瞻性的对照研究证实了晚期肝癌成功转化后手术切除的价值。这也为晚期肝癌的系统治疗的疗效提升提供了可行的方案。绝大部分晚期患者无法被系统治疗所治愈(5 年生存率~20%),如果患者在治疗有效时接受适时的手术切除,则可以争取无瘤生存的机会,进而可能转变成长期生存的机会。
TALENTop 为转化治疗领域的研究提供了一个基本框架,后续的研究和临床实践可以在此基础上进一步优化。在临床工作中,可根据患者的实际情况,选择合适的转化治疗方案(例如考虑增加局部治疗),根据患者的治疗反应调整转化治疗的时长,手术后的续贯治疗都可以根据患者的治疗反应做相应调整。
对于晚期肝癌患者,在缺少生物标志物指导治疗方案选择时,我们还是根据其对系统治疗的反应动态调整治疗策略:
- 对于对系统治疗获益有限的患者,可考虑增加按需的局部治疗(TACE/HAIC/外放射治疗),以推迟一线治疗的失败时间,避免让患者过早进入二线治疗,因为二线治疗的选择非常有限。
- 对于治疗有效的患者,如果获得了手术切除机会,可以考虑增加手术切除,以让患者达到无瘤(NED)状态,并且可以避免其在持续用药中出现治疗耐药。
这种根据治疗反应按需调整治疗方案的策略可能为更多晚期患者赢得长期生存的机会,也许,5 年 OS 率可以提高到 30% 以上?